炭酸脱水酵素
炭酸脱水酵素の構造と機能
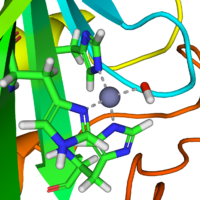
自然界の炭酸脱水酵素は幾つかの形態が存在する。もっとも研究されているものが「α-炭酸脱水酵素」で動物の体内に存在する。亜鉛イオンは His94, His96そしてHis119である3つのヒスチジン残基のイミダソール環が配位している。
動物においてこの酵素の主たる機能は、二酸化炭素と炭酸水素イオンとを相互変換することで、血液や他の組織の酸-塩基平衡を維持し、組織から二酸化炭素を運び出す補助をする。
植物においては「β-炭酸脱水酵素」と呼ばれる形態の異なる酵素が含まれる。その酵素は進化的には起源を異にするが、同じ反応に関与し、活性中心には亜鉛イオンが存在する。植物において炭酸脱水酵素はCO2濃度の上昇を補助し、葉緑体中でリブロース1,5-ビスリン酸カルボキシラーゼ/オキシゲナーゼ酵素の炭酸固定反応を増大させている。この反応により光合成ではCO2ガスを有機化合物の糖に固定しているが、CO2の炭素のみが利用され、炭酸や炭酸水素イオンでは利用されない。
2000年にはカドミウム含有炭酸脱水酵素が亜鉛が限定される海洋の珪藻から発見されている。大洋では亜鉛はその濃度は定常的に低い濃度であり、珪藻のような植物プランクトン生育の制限になりうる。そうした場合、炭酸脱水酵素は環境中で使用できる他の金属イオンを利用する。この発見以前は一般にはカドミウムは生物学的な機能がない非常に毒性のある重金属であると考えられていた。2005年の時点では炭酸脱水酵素に結合する例だけがカドミウムが関与する生化学反応である。
炭酸脱水酵素は次の反応を触媒する。
炭酸脱水酵素の反応速度はすべての酵素の中でも早いもののひとつであり、通常、反応速度の足かせとなるのは基質(二酸化炭素)の拡散速度である。逆反応は相対的に遅い(速度定数は15秒程度である)。炭酸飲料が栓をあけたときにカンやビンでは速やかにガスが抜けずに、口に入れると急にガスが抜けるのは、唾液中に炭酸脱水酵素が含まれるためである。
反応機構
酵素の補欠分子族である亜鉛は3部位のヒスチジン側鎖に配位している。4つ目の配位座は水分子により占められている。水素-酸素結合は分極を生じ、酸素はわずかに陰性を帯びそれにより弱められている。
4番目のヒスチジンが近づくと基質の水からプロトンを受け取る。この例は典型的な酸-塩基触媒モデルである。そして亜鉛から水酸化物イオンが解離する。
活性部位も二酸化炭素に特異的なくぼみを持ち、水酸化物イオンを導入するのに都合が良い。この電子過剰の水酸化物イオンが二酸化炭素に攻撃を加え、炭酸水素イオンが生成する。
炭酸脱水酵素ファミリー
炭酸脱水酵素には少なくとも5つの独立したファミリー (α, β, γ, δそして ε)が存在する。3つのファミリーは.アミノ酸配列にほとんど相同性はなく、平行進化が顕著に現れた例と考えられている。
α-CA
この炭酸脱水酵素は哺乳類から発見され、4つのサブグループに区分されている。
- 細胞質性炭酸脱水酵素群 (CA-I, CA-II, CA-III, CA-VII and CA XIII)
- ミトコンドリア性炭酸脱水酵素群(CA-VA and CA-VB)
- 分泌型炭酸脱水酵素群(CA-VI)
- 膜結合型炭酸脱水酵素群 (CA-IV, CA-IX, CA-XII, CA-XIV and CA-XV)
β-CA
真正細菌と植物の葉緑体に存在する炭酸脱水酵素はβファミリーに属する。このファミリーは次に示す2種類の配列モチーフにより同定される。
- C-[SA]-D-S-R-[LIVM]-x-[AP]
- [EQ]-[YF]-A-[LIVM]-x(2)-[LIVM]-x(4)-[LIVMF](3)-x-G-H-x(2)-C-G
γ-CA
γクラスファミリーの炭酸脱水酵素はメタン菌(メタンを生産する古細菌)より見出されている。
δ-CA
δクラスの炭酸脱水酵素は珪藻より見出された。この区分は最近のもので、独立であるか疑問ももたれている。
ε-CA
εクラスの炭酸脱水酵素は化学合成無機栄養細菌やCSO-Carboxysome を持つ海洋の藍色細菌などの細菌にのみ見出される。 最近の3次元解析によるとε-炭酸脱水酵素は、特に金属イオンサイト部位で、部分的にβ-炭酸脱水酵素と類似性をもつことが示唆されている。しかしこの二つのファミリーはかけ離れており、アミノ酸配列の点ではかなりかけ離れている。
炭酸
炭酸(たんさん、英: carbonic acid)は、化学式 H2CO3 で表される炭素のオキソ酸であり弱酸の一種である。
炭酸 識別情報 CAS登録番号 463-79-6 ChemSpider 747 KEGG C01353 ChEMBL CHEMBL1161632 特性 化学式 H2CO3 モル質量 62.03 g/mol 密度 1.0 g/cm3 (希薄溶液) 融点 n/a
水への溶解度 溶液中にのみ存在 酸解離定数 pKa 6.352 (pKa1) 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 性質
普通は水溶液(炭酸水)中のみに存在し、水に二酸化炭素を溶解(炭酸飽和)することで生じる。
水に溶解した二酸化炭素の一部は水分子の付加により炭酸となる。
この反応の平衡定数 (Kh) は 25 ℃で 1.7 × 10−3 であり、著しく左に偏っているため水溶液中の二酸化炭素の大部分は CO2 分子として存在する。触媒が存在しない場合、二酸化炭素と炭酸の間の反応が平衡に達する速度は低く、正反応の速度定数は 0.039 s−1、逆反応の速度定数は 23 s−1 である。
二酸化炭素と炭酸の平衡は体液の酸性度を調節する上で非常に重要であり、ほとんどの生物はこれら2つの化合物を変換させるための炭酸脱水酵素を持っている。この酵素は反応速度をおよそ10億倍にする。
炭酸は水溶液中で2段階の解離を起こす。25 ℃における酸解離定数は1段階目が pKa1 = 3.60、2段階目が pKa2 = 10.25 であり、炭酸は真の解離定数において酢酸よりも強い酸であるが、上記の二酸化炭素との平衡が存在するために、見かけ上の pKa* が高い非常に弱い酸である。このため炭酸塩は相応の塩基性を示し、灰汁として古代より日常生活のアルカリとして洗浄などに活用されてきた。
酸解離に関する標準エンタルピー変化、ギブス自由エネルギー変化、エントロピー変化の値が報告されており、解離に伴いエントロピーの減少がおこるのは、電荷の増加に伴いイオンの水和の程度が増加し、電縮が起こり水分子の水素結合による秩序化の度合いが増加するからである。この値は以下の平衡に対するものでpKa1*は見かけの酸解離定数である。
,
,
第一解離 7.64 kJ mol−1 36.34 kJ mol−1 −96.3 J mol−1K−1 −377 J mol−1K−1 第二解離 14.85 kJ mol−1 58.96 kJ mol−1 −148.1 J mol−1K−1 −272 J mol−1K−1 不安定性
長い間、炭酸そのものを室温で単離することは不可能だと考えられていた。しかし、1991年にNASA・ゴダード宇宙飛行センターの科学者が初めて純粋な H2CO3 を作り出すことに成功した。彼らは凍結させた水と二酸化炭素に高エネルギーの放射線を照射したのち、加温して余分な水を取り除くことにより単離を行った。得られた炭酸の構造は赤外分光法によって検討された。宇宙空間には水や二酸化炭素の氷が普通に存在することから、この実験結果は宇宙線や紫外線によってそれらが反応することで生成した炭酸も宇宙空間には存在する可能性があることを示唆している。
理論計算によって、水が1分子でも存在すると炭酸はすぐに二酸化炭素と水に戻ってしまうが、水を含まない純粋な炭酸は気体状態で安定であることが示されており、その半減期はおよそ18万年であると見積もられている。
炭酸と雨水
大気中の二酸化炭素 (0.033 %) が溶け込んだ水の pH は 5.6 である。通常の雨水は二酸化炭素で飽和状態になってはいないため、大気汚染物質がなければその pH は 6 前後である。これは二酸化硫黄などの工業廃棄物によって雨水の pH が激しく低下する酸性雨現象とは異なる。しかし、雨の酸性度はチョークや石灰岩などの炭酸塩鉱物に関する重要な地質学的問題である。岩石に含まれる炭酸カルシウムと炭酸水素カルシウムの間には、以下のような溶液中での平衡が成り立っている。
これにより、水が入りこんだ断層線付近の地下洞窟が浸食されることがある。カルシウムを多く含んだ水が蒸発すると炭酸カルシウムが沈殿し、しばしば鍾乳石や石筍を形成する。チョークからなる帯水層からくみ上げられた水は多量の炭酸カルシウムが溶解しており、「硬水」と呼ばれる。
ハイボール
ハイボール (Highball) とはカクテルの一種。広義ではスピリッツ、リキュールをソーダやトニックウォーターなどの炭酸飲料や、フレッシュジュースなどアルコールの含まれていない飲料で割ったものを指す。日本ではウイスキーをソーダ水で割ったもの(ウイスキー・ソーダ)をこう呼ぶのが一般的。
概要
語源については諸説ある。
- 開拓時代のアメリカにおいて、蒸気機関車による長距離移動の時に、途中で水の補給のための停車の際、棒の先にボールをつけたものを掲げて合図した。その時に、バーボンのソーダ割りのサービスがあったことから。
- 同じくアメリカの鉄道で、ボール信号というのが一般的に使用されていた。ボールがあがっていれば進行 (go)、あがっていなければ停止 (don't go) である。駅員が隣の駅のボール信号を望遠鏡で見ながらバーボンをチビチビやっている時にボールが上がったら(ボールがハイになったら)列車が来るというので、ソーダ水を入れて一気に飲み干して駅に行ったというのが語源という説。
- イギリスのゴルフ場のカウンターでウイスキーを飲んでいた人が、急に自分の打つ順が来たことを知らされ、慌ててそばにあったチェイサーにウイスキーをあけ飲んだところ非常においしかった。そこに、たまたまハイ・ボール(高く打ち上がったゴルフボール)が飛んできたから。
- 炭酸の泡(玉)が上に揚がっていく様から、列車のボール信号と掛けて、早く飲み干し、出来上がる、出掛ける、といった洒落。
バーテンダー発祥地(アメリカ)のバーテンダー養成学校では、1または2で言及されている「ボール信号」が語源になっていると教えている。一方、サントリーは公式サイトで諸説のうち3が一番有名な説だと述べている。
脚注
- ^「ハイボール」の名前の由来を教えてください。 サントリーお客様センター(サントリー、2017年3月10日閲覧)
関連項目
ガリガリガリクソンさん 乙ですヾ(╹◡╹o)ノ










![K_{{a1}}={\frac {[{\mbox{H}}^{+}][{\mbox{HCO}}_{3}^{-}]}{[{\mbox{H}}_{2}{\mbox{CO}}_{3}]}}=2.5\times 10^{{-4}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/db3d52a848e9718ad7edbfc0b64dd7c31aa8d37a)



![K_{{a1}}^{*}={\frac {[{\mbox{H}}^{+}][{\mbox{HCO}}_{3}^{-}]}{[{\mbox{H}}_{2}{\mbox{CO}}_{3}]+[{\mbox{CO}}_{2}]}}=4.45\times 10^{{-7}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1c747823775b3471c53f0dd9e49830c176b2acbd)
![K_{{a2}}={\frac {[{\mbox{H}}^{+}][{\mbox{CO}}_{3}^{{2-}}]}{[{\mbox{HCO}}_{3}^{-}]}}=4.7\times 10^{{-11}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c019d2460b9b31ba2498924a72c759151cfd3a8d)







